28 september 2001, Pharmaceutisch Weekblad, Jaargang 136 Nr 39
Bij opname in het wettelijk verzekerde geneesmiddelenpakket beoordeelt het ministerie van Volksgezondheid, Welzijn en Sport (VWS) geneesmiddelen op hun therapeutische vervangbaarheid ten opzichte van andere geneesmiddelen. Geneesmiddelen die als therapeutisch uniek worden beoordeeld, plaatst het ministerie op Bijlage 1b van de Regeling Farmaceutische Hulp. De kosten van de geneesmiddelen die op deze bijlage vermeld staan, krijgt de patiënt volledig vergoed van de zorgverzekeraar. Sinds 1999 plaatst het ministerie weer nieuwe geneesmiddelen op Bijlage 1b. Voor die tijd hanteerde VWS een tijd lang een zeer restrictief toelatingsbeleid voor nieuwe geneesmiddelen. In 2000 is er ƒ 887 miljoen aan dergelijke geneesmiddelen uitgegeven in de openbare apotheek. Dit komt overeen met 13% van de totale geneesmiddelenuitgaven. De SFK verwacht dat in 2001 de uitgaven aan 1b-middelen zullen oplopen tot ƒ 1 miljard (figuur 1). De toename van de uitgaven aan de groep 1b-middelen wordt overigens afgeremd, doordat er regelmatig geneesmiddelen van Bijlage 1b verdwijnen. Dat is het geval zodra er van een therapeutisch uniek geneesmiddel een gelijkwerkende concurrent op de markt komt.
Nieuwere geneesmiddelen
Van alle geneesmiddelenuitgaven heeft 33% betrekking op geneesmiddelen die tien jaar of korter in ons land verkrijgbaar zijn. Bij de 1b-geneesmiddelen bepalen de geneesmiddelen die het afgelopen decennium zijn geïntroduceerd 60% van de uitgaven. De toename van de uitgaven aan 1b-geneesmiddelen vormt een belangrijke indicatie van de extra kosten die voortvloeien uit de therapeutische uitbreiding van het wettelijk verzekerde geneesmiddelenpakket (de kosten van nieuwe geneesmiddelen die als vervanging van bestaande geneesmiddelen kunnen worden gezien daargelaten). Deze toename omvat een volumecomponent - dankzij de nieuwe geneesmiddelentherapieën kunnen er meer patiënten behandeld worden - en een prijscomponent. Het ontwikkelen van een nieuw geneesmiddel is een kostbare aangelegenheid. Als het geneesmiddel gericht is op een beperkte groep patiënten, kan dit tot hoge geneesmiddelenprijzen leiden. Bovendien verkeert de aanbieder van een therapeutisch uniek geneesmiddel in een gunstige concurrentiepositie.
Een 1b-geneesmiddel kost gemiddeld ƒ 2,44 per DDD (Defined Daily Dose, standaard dagdosering die de Wereld Gezondheidszorgorganisatie vaststelt per geneesmiddel). Dit is bijna twee keer zoveel als de gemiddelde kosten per standaard dagdosering bij de overige geneesmiddelen.
Specialisten
Medisch specialisten schrijven verhoudingsgewijs vaker 1b-geneesmiddelen voor dan huisartsen. Van de geneesmiddelen die op voorschrift van een huisarts zijn verstrekt is 6% (uitgedrukt in DDD’s) een 1b-geneesmiddel. Bij medisch specialisten gaat het om ruim 10% van de door hen voorgeschreven geneesmiddelen. De patiëntenpopulatie van een medisch specialist is vanzelfsprekend niet vergelijkbaar met de patiëntenpopulatie van een huisarts.
Grote diversiteit
Binnen de groep geneesmiddelen die vermeld staan op Bijlage 1b werd in 2000 het meeste geld uitgegeven aan geneesmiddelen die gericht zijn op het centraal zenuwstelsel (waaronder het migrainemiddel sumatriptan (ƒ 31 miljoen), het opioïde fentanyl (ƒ 25 miljoen) en diverse antiepileptica), aan antimicrobiëlemiddelen voor systemisch gebruik (waaronder diverse AIDS-middelen (ƒ 75 miljoen)), aan oncolytica en immunomodulantia (waaronder interferon beta te gebruiken bij multiple sclerose (f 65 miljoen)), aan geneesmiddelen gericht op het ademhalingsstelsel (waaronder het CARA-middel ipratropium (ƒ 53 miljoen) en aan dermatologica (waaronder terbinafine te gebruiken bij kalknagels (ƒ 52 miljoen)).
Figuur 1: uitgaven aan geneesmiddelen die geplaatst zijn op Bijlage 1b van de Regeling Farmaceutische Hulp
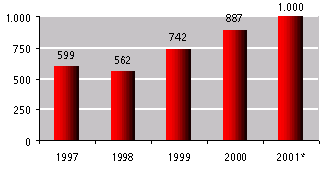
Bron: Stichting Farmaceutische Kengetallen
Figuur 2: uitgaven aan 1b-geneesmiddelen naar anatomie

Bron: Stichting Farmaceutische Kengetallen
Dit is een publicatie van de Stichting Farmaceutische Kengetallen.
Overname van tekst, gegevens, tabellen of grafieken is toegestaan mits
onder volledige bronvermelding.